Bakır (I) siyanür - Copper(I) cyanide - Wikipedia
 | |
| İsimler | |
|---|---|
| IUPAC adı Bakır (I) siyanür | |
| Diğer isimler Bakır siyanür, bakır siyanür, kuprisin | |
| Tanımlayıcılar | |
3 boyutlu model (JSmol ) | |
| ChemSpider | |
| ECHA Bilgi Kartı | 100.008.076 |
| EC Numarası |
|
PubChem Müşteri Kimliği | |
| RTECS numarası |
|
| UNII | |
| BM numarası | 1587 |
CompTox Kontrol Paneli (EPA) | |
| |
| |
| Özellikleri | |
| CuCN | |
| Molar kütle | 89,563 g / mol |
| Görünüm | kirli beyaz / soluk sarı toz |
| Yoğunluk | 2,92 g / cm3[1] |
| Erime noktası | 474 ° C (885 ° F; 747 K) |
| önemsiz | |
| Çözünürlük | içinde çözülmez etanol, soğuk seyreltik asitler; içinde çözünür NH4OH, KCN, ve DMF |
| -24.0·10−6 santimetre3/ mol | |
| Yapısı | |
| monoklinik | |
| Tehlikeler | |
| Güvenlik Bilgi Formu | Oxford MSDS |
| GHS piktogramları |   |
| GHS Sinyal kelimesi | Tehlike |
| H300, H310, H330, H400, H410 | |
| P260, P262, P264, P270, P271, P273, P280, P284, P301 + 310, P302 + 350, P304 + 340, P310, P320, P321, P322, P330, P361, P363, P391, P403 + 233, P405, P501 | |
| NFPA 704 (ateş elması) | |
| Alevlenme noktası | Yanıcı değil |
| NIOSH (ABD sağlık maruziyet sınırları): | |
PEL (İzin verilebilir) | TWA 1 mg / m23 (Cu olarak)[2] |
REL (Önerilen) | TWA 1 mg / m23 (Cu olarak)[2] |
IDLH (Ani tehlike) | TWA 100 mg / m3 (Cu olarak)[2] |
Aksi belirtilmedikçe, veriler kendi içlerindeki malzemeler için verilmiştir. standart durum (25 ° C'de [77 ° F], 100 kPa). | |
| Bilgi kutusu referansları | |
Bakır (I) siyanür bir inorganik bileşik CuCN formülü ile. Bu kirli beyaz katı ikide oluşur polimorflar; saf olmayan numuneler, Cu (II) safsızlıklarının varlığından dolayı yeşil olabilir. Bileşik, bir katalizör, galvanik bakırda ve bir reaktif hazırlanmasında nitriller.[3]
Yapısı
Bakır siyanür bir koordinasyon polimeri. Her ikisi de - [Cu-CN] - ile bağlanan doğrusal bakır (I) merkezlerinden yapılmış zincirler içeren iki polimorfta bulunur. siyanür köprüler. Yüksek sıcaklık polimorfunda, HT-CuCN ile izostrüktürel AgCN Doğrusal zincirler altıgen bir kafes üzerinde paketlenir ve bitişik zincirler +/- 1/3 olarak ayarlanır. c, Şekil 1.[4] Düşük sıcaklık polimorfu LT-CuCN'de, zincirler doğrusallıktan sapar ve 49 ° döndürülen bitişik katmanlardaki zincirlerle AB tarzında paketlenen dalgalı katmanlara paketlenir, Şekil 2.[5]
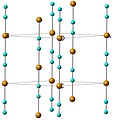
Şekil 1: c ekseni boyunca ilerleyen zincirleri gösteren HT-CuCN yapısı. Anahtar: bakır = turuncu ve camgöbeği = baştan sona düzensiz siyanür grupları.

Şekil 2: Bir ABAB tarzında istiflenen zincir tabakalarını gösteren LT-CuCN yapısı. Anahtar bakır = turuncu ve camgöbeği = baştan sona düzensiz siyanür grupları.
LT-CuCN, inert bir atmosferde 563 K'ye ısıtılarak HT-CuCN'ye dönüştürülebilir. Her iki polimorfta da bakırdan karbona ve bakırdan nitrojene bağ uzunlukları ~ 1.85 A'dır ve köprü siyanür grupları baştan sona bozukluk gösterir.[6]
Hazırlık
Bakır siyanür ticari olarak mevcuttur ve düşük sıcaklık polimorfu olarak sağlanır. İndirgenerek hazırlanabilir bakır (II) sülfat 60 ° C'de sodyum hidrojensülfit ile, ardından eklenmesi sodyum siyanür saf LT-CuCN'yi soluk sarı bir toz olarak çökeltmek için.[7]
- 2 CuSO4 + NaHSO3 + H2O + 2 NaCN → 2 CuCN + 3 NaHSO4
Sodyum bisülfit ilavesiyle bakır sülfat çözeltisi maviden yeşile döner ve bu noktada sodyum siyanür eklenir. Reaksiyon, hafif asidik koşullar altında gerçekleştirilir. Bakır siyanür tarihsel olarak bakır (II) sülfatın sodyum siyanür ile işlenmesiyle hazırlanmıştır, bu redoks reaksiyonunda bakır (I) siyanür ile birlikte disiyan:[8]
- 2 CuSO4 + 4 NaCN → 2 CuCN + (CN)2 + 2 Na2YANİ4
Bu sentetik yol disiyan ürettiğinden, yapılan CuCN eşdeğeri başına iki eşdeğer sodyum siyanür kullandığından ve elde edilen bakır siyanür saf olmadığından, endüstriyel üretim yöntemi değildir. Bakır (I) iyodür oluşturmak için bu reaksiyonun bakır sülfat ve sodyum iyodür arasındaki benzerliğe benzerliği, sözde halojenür olarak hareket eden siyanür iyonlarının bir örneğidir. Ayrıca neden bakır (II) siyanür, Cu (CN)2, sentezlenmedi.
Tepkiler
Bakır siyanür suda çözünmez ancak CN içeren çözeltilerde hızla çözünür.− oluşturmak için [Cu (CN)3]2− ve [Cu (CN)4]3−, sırasıyla trigonal düzlemsel ve dört yüzlü koordinasyon geometrisi sergileyen. Bu kompleksler, [M (CN) oluşturan gümüş ve altın siyanürlerle tezat oluşturuyor.2]− çözelti içindeki iyonlar.[9] Koordinasyon polimeri KCu (CN)2 [Cu (CN) içerir2]− sarmal anyonik zincirler oluşturan birbirine bağlanan birimler.[10]
Bakır siyanür ayrıca konsantre sulu amonyak, piridin ve N-metilpirolidon içinde çözünür.
Başvurular
Bakır siyanür, bakırın elektrokaplamasında kullanılır.[3]
Organik sentez
CuCN önde gelen bir reaktiftir organo-bakır kimyası. Tepki verir organolityum reaktifleri Li [RCuCN] ve Li formülleri ile "karışık bakır oranlar" oluşturmak için2[R2CuCN]. CuCN kullanımı, CuR ve LiCuR tipi daha basit organo-bakır reaktiflerin dağıtımında devrim yarattı2, Gilman reaktifleri. Siyanür varlığında, bu karışık bakır oranlar daha kolay saflaştırılır ve daha kararlıdır.
Karışık bakır oranları Li [RCuCN] ve Li2[R2CuCN], karbanyonların kaynağı olarak işlev görür R−, ancak ana organolityum reaktifine kıyasla azaltılmış reaktiviteye sahiptir. Bu nedenle, eşlenik eklemeler ve bazı yer değiştirme reaksiyonları için faydalıdırlar. CuCN'nin eklenmesi[açıklama gerekli ] [11]
CuCN ayrıca R kaynakları olarak kullanılan silil ve stannil reaktifleri oluşturur.3Si− ve R3Sn−.[12]
CuCN, aril halojenürlerin nitrillere dönüştürülmesinde kullanılır.[11]
Referanslar
- ^ Lide, David R., ed. (2006). CRC El Kitabı Kimya ve Fizik (87. baskı). Boca Raton, FL: CRC Basın. ISBN 0-8493-0487-3.
- ^ a b c Kimyasal Tehlikeler için NIOSH Cep Rehberi. "#0150". Ulusal Mesleki Güvenlik ve Sağlık Enstitüsü (NIOSH).
- ^ a b H. Wayne Richardson "Bakır Bileşikleri" Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2005. doi:10.1002 / 14356007.a07_567
- ^ S. J. Hibble; S. M. Cheyne; A. C. Hannon; S. G. Eversfield (2002). "CuCN: Polimorfik Matirial. Toplam Nötron Kırınımından Bir Formun Yapısı". Inorg. Chem. 41 (20): 8040–8048. doi:10.1021 / ic0257569.
- ^ S. J. Hibble; S. G. Eversfield; A. R. Cowley; A. M. Chippindale (2004). "Bakır (I) Siyanür: Karmaşık Bir Yapıya ve Şaşırtıcı Oda Sıcaklığı Reaktivitesine Sahip Basit Bir Bileşik". Angew. Chem. Int. Ed. 43 (5): 628–630. doi:10.1002 / anie.200352844.
- ^ S. Kroeker; R. E. Wasylishen; J. V. Hanna (1999). "Katı Bakır (I) Siyanürün Yapısı: Çok Çekirdekli Manyetik ve Kuadropol Rezonans Çalışması". Amerikan Kimya Derneği Dergisi. 121 (7): 1582–1590. doi:10.1021 / ja983253p.
- ^ H. J. Barber (1943). "Bakırlı Siyanür: Hazırlanması ve Kullanımı Hakkında Bir Not". J. Chem. Soc.: 79. doi:10.1039 / JR9430000079.
- ^ J. V. Supniewski ve P.L. Salzberg (1941). "Alil Siyanür". Organik Sentezler.; Kolektif Hacim, 1, s. 46
- ^ Sharpe, A.G. (1976). Geçiş Metallerinin Siyano Komplekslerinin Kimyası. Akademik Basın. s. 265. ISBN 0-12-638450-9.
- ^ Housecroft, Catherine E .; Sharpe, Alan G. (2008) İnorganik Kimya (3. baskı), Pearson: Prentice Hall. ISBN 978-0-13-175553-6
- ^ a b Steven H. Bertz, Edward H. Fairchild, Karl Dieter, "Copper (I) Cyanide", Encyclopedia of Reagents for Organic Synthesis 2005, John Wiley & Sons. doi:10.1002 / 047084289X.rc224.pub2
- ^ Modern Organocopper Kimyasında Dieter, R. K.; Krause, N., Ed .; Wiley-VCH: Mörlenback, Almanya, 2002; Bölüm 3.



